
مواد
- مراحل
- طریقہ 1 آزمائشی اور غلطی کے طریقہ کار کے ذریعہ مساوات کا توازن رکھنا
- طریقہ نمبر 2 الجبری طریقہ کے ذریعہ ایک مساوات کو ہم آہنگ کریں
کیمیا میں ، ایک مساوات قائم کرتا ہے جو کیمیائی رد عمل کے دوران ہوا تھا۔ مساوات کے بائیں طرف ، ہم تجربے کے دوران استعمال ہونے والی اشیا کو دائیں اور دائیں طرف رکھ دیتے ہیں۔ کیمیائی رد عمل کے دوران بڑے پیمانے پر (Lavoisier) کے تحفظ کے اصول کے مطابق ، کوئی ایٹم غائب نہیں ہوتا ہے ، کوئی بھی پیدا نہیں ہوتا ہے ، وہ مختلف طرح سے مل جاتے ہیں۔ خلاصہ یہ کہ آپ کے پاس دائیں جانب ہر عنصر کے ایک جیسے اعدادوشمہ مساوات کے بائیں جانب ہونا ضروری ہے۔ یہی وجہ ہے کہ ایک متوازن مساوات ہمیشہ متوازن ہونا چاہئے۔
مراحل
طریقہ 1 آزمائشی اور غلطی کے طریقہ کار کے ذریعہ مساوات کا توازن رکھنا
-
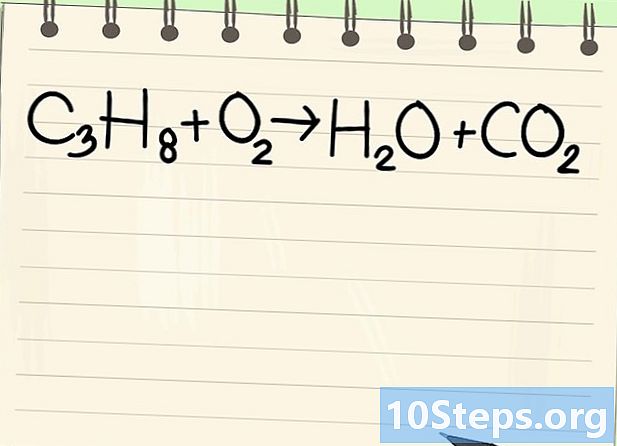
بیلنس مساوات کو نوٹ کریں۔ ہم مندرجہ ذیل مساوات کا علاج کریں گے۔- C3H8 + O2 -> ایچ2O + CO2
- یہ پروپین دہن (سی3H8) آکسیجن میں: پانی اور کاربن ڈائی آکسائیڈ حاصل کیا جاتا ہے۔
-
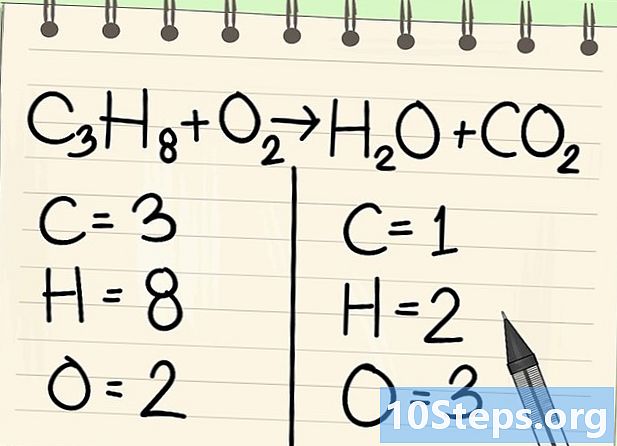
ایٹم گنیں۔ مساوات کے ایک طرف ہر عنصر کے ڈیٹمز کی تعداد درج کریں ، پھر دوسرا۔ اس کے ل the ، فہرستوں کو بھی مدنظر رکھیں ، اگر کوئی نہیں ہے تو ، انڈیکس 1 ہے۔- بائیں طرف ، 3 کاربن جوہری ، 8 ہائیڈروجن اور 2 آکسیجن ہیں۔
- دائیں طرف ، کاربن کا 1 ایٹم ، ہائیڈروجن کا 2 اور آکسیجن کا 3 ہے۔
-
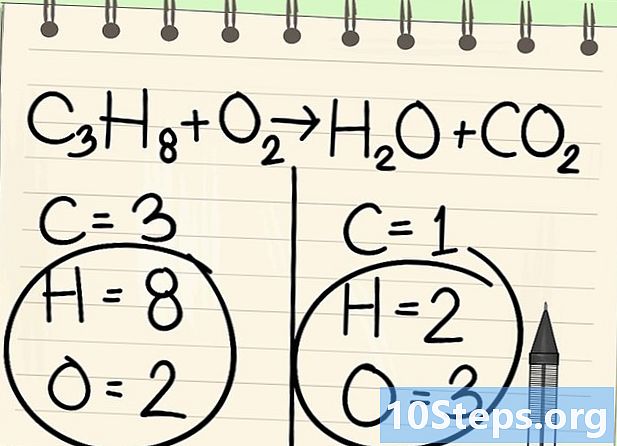
ہائیڈروجن اور آکسیجن کو لمحہ بہ لمحہ ایک طرف چھوڑ دیں۔ -

صحیح عنصر کے ساتھ توازن شروع کریں۔ ہم ہمیشہ اس سے پہلے اور اس کے بعد انوے میں سے ایک کے ساتھ آغاز کرتے ہیں۔ اگر وہاں بہت سے ہیں تو ، انووں میں سے ایک میں monovalent ہے کہ ایک لے لو. یہاں ہم کاربن جوہری سے شروع کرتے ہیں۔ -

کاربن جوہری توازن رکھیں۔ ، دائیں طرف ، کاربن ڈائی آکسائیڈ انو (CO2) جس میں کاربن لیٹومیٹ تنہا ہے۔ 3 بائیں ایٹم حاصل کرنے کے لئے ہم ایک 3 لگائیں گے۔- C3H8 + O2 -> ایچ2O + 3CO2
- اس طرح ہمارے پاس 3 کاربن جوہری صحیح تعداد (3CO) کی بدولت ہیں2) اور بائیں طرف کاربن کے 3 جوہری انڈیکس (C) کا شکریہ3H8).
- ایک مساوات میں ، آپ اپنے مطلوبہ تمام گتانکیاں لگا سکتے ہیں ، لیکن آپ اشارے کو چھو نہیں سکتے ہیں۔
-
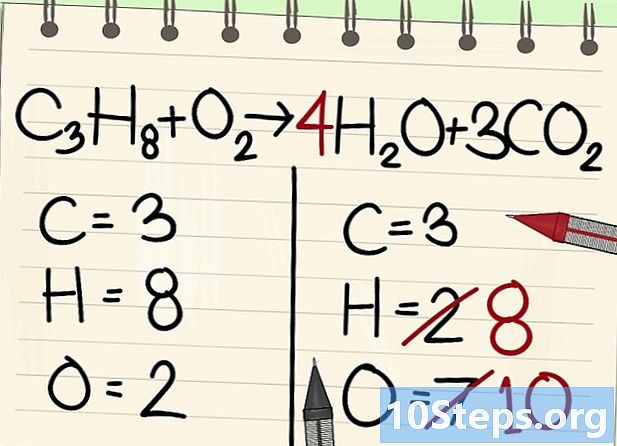
ہائیڈروجن ایٹموں کو متوازن رکھیں۔ چونکہ آپ کے پاس 8 مساوات باقی ہیں ، آپ کو زیادہ سے زیادہ دائیں کی ضرورت ہوگی۔- C3H8 + O2 --> 4H2O + 3CO2
- دائیں طرف ، آپ 4 کا گتانک لگائیں گے ، کیوں کہ پانی کے انو میں ہائیڈروجن متناسب ہے: انڈیکس 2 اشارہ کرتا ہے کہ دو ہائیڈروجن جوہری منسلک ہیں۔
- دائیں طرف ہائیڈروجن ایٹموں کی تعداد حاصل کرنے کے ل you ، آپ گنجائش 4 کو انڈیکس 2 ، یا 8 ایٹموں سے ضرب کرتے ہیں۔
- جہاں تک آکسیجن کے ایٹموں کی بات ہے تو ، دائیں طرف ، اب ایک طرف 6 ہیں ، جو 3CO کے تین انووں سے آرہے ہیں2 (3 x 2 = 6 جوہری) اور 4 H کے 4 مالیکیولوں میں سے 42O (4 x 1 = 4 جوہری) ، یعنی آکسیجن کے کل 10 جوہری۔
-
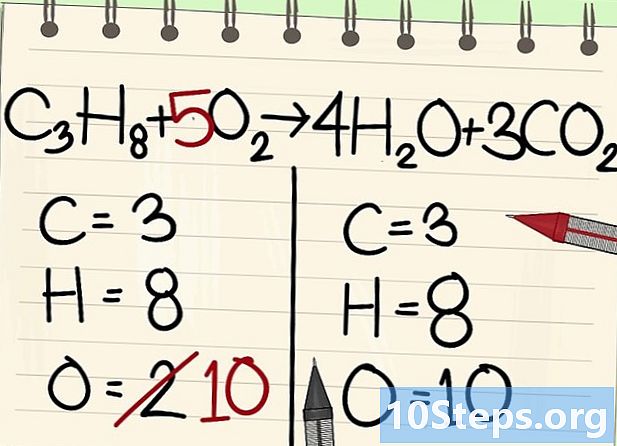
آکسیجن کے جوہری توازن۔- کاربن اور ہائیڈروجن توازن کی وجہ سے ، مساوات کے دونوں اطراف میں آکسیجن ایٹموں کی تعداد ایک جیسی نہیں ہے۔ ہم نے پہلے دیکھا کہ دائیں طرف آکسیجن کے 10 ایٹم موجود تھے (پانی کے انووں سے 4 ، اور 6 کاربن ڈائی آکسائیڈ انووں سے)۔ بائیں طرف ، صرف 2 (O سے) ہیں2).
- آکسیجن کو متوازن کرنے کے لئے ، بائیں آکسیجن انو میں 5 کا ایک گتانک شامل کریں: آپ کے پاس بائیں طرف آکسیجن کے 10 جوہری ہیں اور دوسرا دائیں طرف۔
- C3H8 + 5اے2 -> 4 ایچ2O + 3CO2
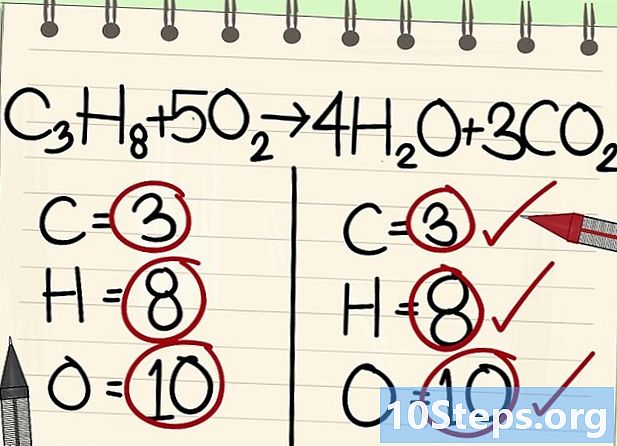
- تمام ایٹم (کاربن ، ہائیڈروجن اور آکسیجن) متوازن ہیں: آپ کا مساوات متوازن ہے۔
طریقہ نمبر 2 الجبری طریقہ کے ذریعہ ایک مساوات کو ہم آہنگ کریں
-

متوازن کرنے کے لئے مساوات لکھیں. ہر انو کو لفظی قابلیت تفویض کریں۔ ہم ان کو فون کریں گے ہے, ب, ج اور ڈی. -
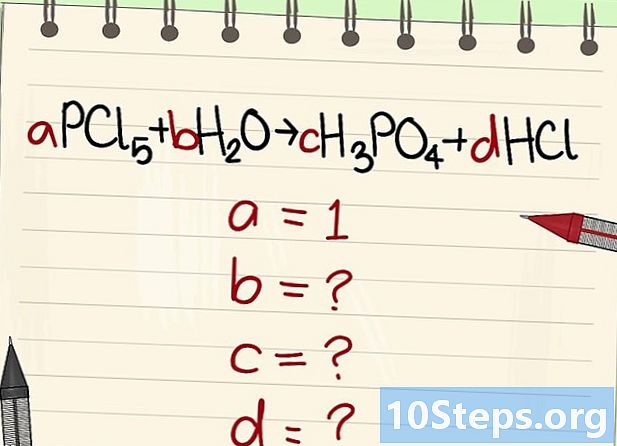
دوسرے لغوی صابن کی قدر معلوم کریں۔ ہم یہ پوچھیں گے ہے = 1. -

ان کوفیفیئنٹ کے درمیان تعلقات تلاش کریں۔ بائیں (ری ایجنٹس) اور دائیں (مصنوعات) کی تلاش کرتے ہوئے ، ان مختلف قابلیت کے درمیان تعلقات قائم کریں۔- مندرجہ ذیل مساوات لیں: aPCl5 + bH2O = cH3PO4 + dHCl. یہ بتایا گیا ہے کہ a = 1 ، جس کا مطلب ہے کہ c = a، d = 5a اور 2b = 3c + d۔ حساب کتابیں ، c = 1 ، d = 5 اور b = 4۔

- مندرجہ ذیل مساوات لیں: aPCl5 + bH2O = cH3PO4 + dHCl. یہ بتایا گیا ہے کہ a = 1 ، جس کا مطلب ہے کہ c = a، d = 5a اور 2b = 3c + d۔ حساب کتابیں ، c = 1 ، d = 5 اور b = 4۔


